弱毒化した病原体または病原体の特定のタンパク質を精製して使用する従来のワクチン製造は、時間を要する複雑なプロセスである。一方、核酸ワクチンは、容易に抗原を作り変えられるほか、安全性も高い。DNAワクチンには、細胞のゲノムに組み込まれる危険性や、抗DNA抗体が産生される危険性がある。そのため、RNAワクチンの優位性は明白であり、より安全と考えられる。
しかし、メッセンジャーRNA(mRNA)は十分な免疫応答を引き出し、抗原提示細胞(APC)を活性化することができない(免疫の賦活化)。これはワクチンがその効果を発揮する上で非常に重要なステップである。複数の試験ではアジュバントと呼ばれる免疫賦活化物質が使われているが、従来の病原体由来ワクチンで用いられたアジュバントが転用されており、mRNAワクチンの特性を踏まえたアジュバント開発は行われてこなかった。そこで、日本の研究者らは、効果的な免疫応答を引き出すことができる安全かつ有効なmRNAワクチンアジュバントの開発に取り組んだ。
川崎市産業振興財団、ナノ医療イノベーションセンター(iCONM)の位髙啓史主幹研究員、内田智士客員研究員と、東京大学、東京医科歯科大学および大阪府立大学の研究者らは、免疫賦活化作用が強い2本鎖(ds)RNA構造をmRNAに組み込むことで、アジュバント機能を一体化させた。dsRNA(mRNA:pU)は、mRNAと、mRNAのポリA部に相補的なRNA鎖構造で構成される。このような設計によって、in vitroで細胞株および骨髄由来APCにおいて強い免疫刺激が得られた。また、マウスにmRNA:pUを注射すると、1本鎖mRNAと比してより効率的に細胞性および液性免疫応答が誘導された。
このように研究者らは、mRNAからの抗原タンパク質の翻訳活性を保ったまま、強い免疫賦活化作用を得ることに成功した。また、これまでmRNAが導入されるAPCを活性化することが課題であったが、今回mRNA:pU自体がアジュバントとして機能するため、この点が担保される。したがって、mRNA:pU自体をアジュバントとして機能させたことは、極めて重要なポイントである。mRNA:pUはRNA分子のみで構成されるため、従来のワクチンアジュバントに優る利点がある。RNAは通常、投与後数日で分解されるため、長期的な蓄積の危険性がないのだ。
「新規のmRNA:pUは、目的や経路に応じてさまざまなmRNAキャリアを用いて送達できるため、mRNAワクチンの効果向上に向けた汎用プラットフォームとなる」と著者らは結論している。
Publication and Affiliations:
Satoshi Uchida a, b, *, Naoto Yoshinaga a, b, Kayoko Yanagihara b, c, Eiji Yuba d, Kazunori Kataoka b, e, Keiji Itaka b, f, *, Designing immunostimulatory double stranded messenger RNA with maintained translational activity through hybridization with poly A sequences for effective vaccination. Biomaterials (2017). DOI: 10.1016/j.biomaterials.2017.09.033
- Department of Bioengineering, Graduate School of Engineering, The University of Tokyo, Bunkyo, Tokyo 113-8656, Japan
- Innovation Center of NanoMedicine, Kawasaki Institute of Industrial Promotion, Kawasaki, Kanagawa 210-0821, Japan
- Division of Clinical Biotechnology, Center for Disease Biology and Integrative Medicine, Graduate School of Medicine, The University of Tokyo, Bunkyo, Tokyo 113-0033, Japan
- Department of Applied Chemistry, Graduate School of Engineering, Osaka Prefecture University, Sakai, Osaka 599-8531, Japan
- Policy Alternatives Research Institute, The University of Tokyo, Bunkyo, Tokyo 113-0033, Japan
- Institute of Biomaterials and Bioengineering, Tokyo Medical and Dental University (TMDU), Chiyoda, Tokyo 101-0062, Japan
* Corresponding authors: E-mail addresses suchida@bmw.t.u-tokyo.ac.jp (S. Uchida), itaka.bif@tmd.ac.jp (K. Itaka).
Figure:
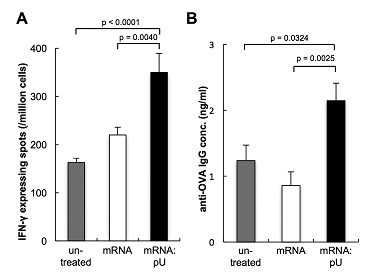
mRNA:pUはin vivoにおいて、1本鎖mRNAに比して高い細胞性免疫応答(A)と抗原産生(B)を引き出す。

